劉 昱1 ,周子丹2 ,伍 洋3 ,張蓬朝1 ,田雨豐2 ,李光強(qiáng)1
(1. 武漢科技大學(xué) 鋼鐵冶金及資源利用省部共建教育部重點(diǎn)實(shí)驗(yàn)室,湖北 武漢 430081;
2. 武漢科技大學(xué) 鋼鐵冶金新工藝湖北省重點(diǎn)實(shí)驗(yàn)室,湖北 武漢 430081;
3.湖北城市建設(shè)職業(yè)技術(shù)學(xué)院,湖北 武漢 430200)
摘 要:綜述了轉(zhuǎn)爐鋼渣的兩種直接碳化方式及其影響因素和動(dòng)力學(xué)機(jī)制,鋼渣的高溫碳化主要限制性環(huán)節(jié)是 CO2穿過(guò)產(chǎn)物層向鋼渣內(nèi)部未反應(yīng)區(qū)域的擴(kuò)散,通過(guò)提高溫度加快 CO2 的擴(kuò)散速率和降低鋼渣顆粒尺寸以減小抑制擴(kuò)散的產(chǎn)物層厚度等措施,可大幅提高鋼渣高溫碳化的固碳量和轉(zhuǎn)化率。濕法碳化的主要限制環(huán)節(jié)是鋼渣中鈣從內(nèi)部向鋼渣表面的擴(kuò)散,降低鋼渣顆粒尺寸和利用超聲波震蕩破壞產(chǎn)物層能有效加快鈣擴(kuò)散浸出。由于鋼渣從轉(zhuǎn)爐出來(lái)后具有較高的溫度,且單一的碳化方式都有其局限,可考慮將兩種固碳方式結(jié)合使用,首先在高溫鋼渣的冷卻過(guò)程中利用鋼渣余熱進(jìn)行高溫干法碳化,并降低鋼渣顆粒尺寸和增加 CO2壓力來(lái)提高固碳量和鈣的轉(zhuǎn)化率;通過(guò)干法碳化固定一部分鈣,而后再進(jìn)行濕法碳化,這樣有利于縮短濕法碳化時(shí)間,待鋼渣高溫碳化結(jié)束經(jīng)冷卻球磨后再進(jìn)行濕法碳化,結(jié)合尺寸優(yōu)化和超聲波的利用,實(shí)現(xiàn)鋼渣最大程度的碳化;該過(guò)程充分利用了鋼渣自身?xiàng)l件,能更有效實(shí)現(xiàn)固碳過(guò)程的節(jié)能減排。
關(guān)鍵詞:轉(zhuǎn)爐鋼渣;高溫干法碳化;濕法碳化;動(dòng)力學(xué);擴(kuò)散
大量化石燃料消耗所產(chǎn)生的 CO2是造成溫室效應(yīng)和全球氣候變暖的主要原因,從工業(yè)革命開(kāi)始,空氣中 CO2的體積分?jǐn)?shù)已經(jīng)從 280´10-6 增加到 415´10-6,并且還在增加[1]。與此同時(shí),自 1880 年以來(lái)全球氣溫已經(jīng)上升約 1.05 ℃,這是世界面臨的最嚴(yán)重的環(huán)境危害[2]。為了避免全球變暖和氣候變化可能造成的破壞性后果,必須大大減少人為活動(dòng)造成的CO2 排放。然而,化石燃料的便捷性及相對(duì)實(shí)惠的市場(chǎng)價(jià)值使得其他的能量來(lái)源暫時(shí)很難將其替代。通過(guò)吸收產(chǎn)生的 CO2減少其排放,即碳的捕捉與存儲(chǔ)技術(shù),是十分有前景的解決途徑[3-4]。最早的固碳方法是通過(guò)地質(zhì)封存,在 20 世紀(jì) 70 年代的采掘工業(yè)中得到了大規(guī)模應(yīng)用,以提高油氣采收率;雖然這種類(lèi)型的儲(chǔ)存可能有足夠的容量,但存在泄漏風(fēng)險(xiǎn)和儲(chǔ)存 CO2的長(zhǎng)期管理問(wèn)題[5]。也有報(bào)道提出將 CO2注入海洋,與水反應(yīng)形成碳酸,達(dá)到海洋固碳的目的,然而,這種方案對(duì)環(huán)境的影響具有不確定性,特別是會(huì)導(dǎo)致海水 pH 值降低且缺乏持久性[4]。
最具前景和可行性的碳捕捉與存儲(chǔ)的技術(shù)方案是由 Seifritz 在 1990 年首次提出的通過(guò)礦物碳化的方式吸收 CO2 [6],并由 Lackner 等人首先進(jìn)行了更為細(xì)致的研究[7]。礦物碳化吸收 CO2的基本原理是模擬自然風(fēng)化過(guò)程,通過(guò)利用含鈣或鎂的礦物吸收 CO2形成碳酸鈣或碳酸鎂來(lái)固定 CO2,如式(1)所示:
(Ca,Mg)SiO3(s)+CO2(g)→(Ca,Mg)CO3(s)+SiO2(s) (1)
相比上述兩種 CO2封存方式,礦物碳化吸收 CO2具有以下潛在優(yōu)勢(shì):其一是礦物碳化是一種化學(xué)固碳方式,產(chǎn)物具有熱力學(xué)穩(wěn)定性,CO2 存儲(chǔ)是永久性的且本質(zhì)上安全可靠;此外,由于碳化反應(yīng)是放熱反應(yīng),固碳過(guò)程能源消耗有限。劣勢(shì)是需要消耗大量的鈣/鎂礦石,但是大量的含鈣/鎂的工業(yè)固廢可以替代礦石用于 CO2的固定,如鋼渣、飛灰等。這些工藝副產(chǎn)品一般是堿性的且富含鈣,與礦石固碳相比具有更低的成本,將其用于固碳也能起到固廢處理及其二次利用的作用。
目前國(guó)內(nèi)多采用氧氣轉(zhuǎn)爐煉鋼工藝,每噸鋼產(chǎn)生100~130 kg的鋼渣。由于需要滿足鋼水脫磷的要求,轉(zhuǎn)爐鋼渣含有較高的 CaO含量,使得鋼渣中含有自由氧化鈣,在水化時(shí)會(huì)導(dǎo)致體積膨脹,這給轉(zhuǎn)爐鋼渣的再利用帶來(lái)困難,大量鋼渣的堆放占用空間,造成土地資源的浪費(fèi),產(chǎn)生的粉塵也會(huì)加大工程環(huán)保壓力、危害人員健康。現(xiàn)有轉(zhuǎn)爐鋼渣處理工藝由于處理成本高、性能多變而導(dǎo)致鋼渣應(yīng)用程度有限。相比之下,通過(guò)對(duì)轉(zhuǎn)爐鋼渣進(jìn)行碳化處理,使鋼渣中的堿性氧化物與 CO2反應(yīng)形成碳酸鹽,不僅可以消除鋼渣中的自由氧化鈣,而且鋼鐵工業(yè)也是 CO2排放大戶,鋼渣固碳可以就近利用 CO2,減少碳排放,碳化處理后的鋼渣可用于混凝土等基礎(chǔ)設(shè)施建設(shè)材料[7-9]。
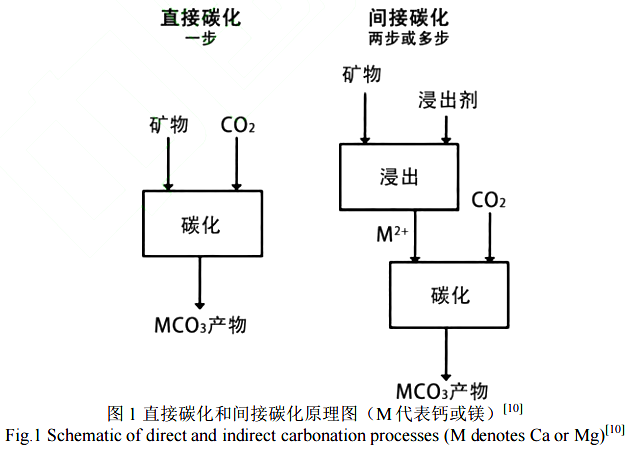
自然風(fēng)化過(guò)程太慢,因此,以礦物碳化方式實(shí)現(xiàn) CO2封存的研究目的是加速反應(yīng),以獲得可行的工業(yè)過(guò)程。目前關(guān)于礦物的碳化主要有兩種方式:直接碳化和間接碳化。如圖1 所示[10],直接碳化是最簡(jiǎn)單的礦物固碳方式,其原理是利用干燥、潮濕或含水的環(huán)境,在單一反應(yīng)步驟中實(shí)現(xiàn)碳酸化;而間接碳化分幾個(gè)步驟實(shí)現(xiàn),包括堿性元素的浸出提取和碳酸化。
關(guān)于利用 CH3COOH 或銨鹽對(duì)鋼渣進(jìn)行間接碳化的研究有很多[11-13],從這些研究工作中可以看出一個(gè)普遍趨勢(shì)是,雖然通過(guò)這些方法可以利用廢棄物生產(chǎn)出有價(jià)值的產(chǎn)品(較高純度的碳酸鈣),但也會(huì)帶來(lái)其他問(wèn)題,包括含有不穩(wěn)定重金屬的殘余固廢,以及含鹽和重金屬的廢水,廢物處理的目標(biāo)并沒(méi)有完全實(shí)現(xiàn)。
相比之下,直接碳化不需要使用浸出溶劑,具備成本優(yōu)勢(shì)[14]。轉(zhuǎn)爐鋼渣的處理主要采用直接碳化的方式進(jìn)行,可分為干法碳化和濕法碳化兩類(lèi)[15]。本文將結(jié)合文獻(xiàn)從熱力學(xué)和動(dòng)力學(xué)角度總結(jié)歸納鋼渣碳化的影響因素及相關(guān)作用機(jī)制,為加快鋼渣碳化、實(shí)現(xiàn)鋼渣再利用及減少碳排放提供理論指導(dǎo)。
1 轉(zhuǎn)爐鋼渣碳化的熱力學(xué)與動(dòng)力學(xué)
轉(zhuǎn)爐鋼渣中含鈣礦物如 f-CaO、C3S、β-C2S 及水化活性低的 γ-C2S 和硅酸鹽(CaSiO3(CS))等均能發(fā)生碳化反應(yīng),這為鋼渣碳化提供了良好的物質(zhì)條件[16]。雖然鋼渣的水化反應(yīng)活性較低,但在富 CO2的環(huán)境下,鋼渣中各種含鈣礦物組分表現(xiàn)出較高的碳化反應(yīng)活性。而在自然條件下,鋼渣碳化緩慢,且過(guò)程比較復(fù)雜。轉(zhuǎn)爐鋼渣碳化主要采用直接碳化,該方法可分為兩類(lèi):干法碳化和濕法碳化。
干法碳化是一個(gè)氣-固反應(yīng)過(guò)程,氣態(tài) CO2直接與渣中堿金屬氧化物反應(yīng)形成碳酸鹽,如式(2)所示[10]:
CaO+CO2→CaCO3 (2)
該反應(yīng)屬于放熱反應(yīng),從鋼渣成分來(lái)看,其在氣-固反應(yīng)固碳方面有著顯著的優(yōu)勢(shì)。但氣-固反應(yīng)固碳的反應(yīng)速率卻相對(duì)較慢,導(dǎo)致較低的固碳量[17-19]。其反應(yīng)動(dòng)力學(xué)過(guò)程符合未反應(yīng)核模型[20],在反應(yīng)初期,其反應(yīng)動(dòng)力學(xué)過(guò)程主要為:1)CO2向氣相/固相反應(yīng)界面擴(kuò)散;2)氣相/固相界面處 CO2氣體與鋼渣中堿金屬氧化物發(fā)生反應(yīng)。此時(shí),一般氣體外擴(kuò)散不是限制性環(huán)節(jié),碳化反應(yīng)速率主要由界面化學(xué)反應(yīng)速率控制。而隨著界面化學(xué)反應(yīng)的發(fā)生,新相碳酸鈣產(chǎn)物層的形成,反應(yīng)過(guò)程包括以下環(huán)節(jié):1)氣體在鋼渣顆粒外的外擴(kuò)散;2)氣體穿過(guò)固相產(chǎn)物層的內(nèi)擴(kuò)散;3)氣體與固體物的界面化學(xué)反應(yīng)。Revathy 等人[21]對(duì)室溫下鋼渣的干法碳化進(jìn)行了研究,發(fā)現(xiàn)碳化過(guò)程可以在室溫下自發(fā)進(jìn)行,在 1 h 的碳化后鋼渣的固碳速率減慢,3 h 后 CO2吸收量幾乎不再增加,這主要是由于鋼渣顆粒表面在碳化過(guò)程中形成的碳酸鹽層以及反應(yīng)后殘余的貧鈣硅酸鹽區(qū)域阻礙了 CO2氣體向鋼渣顆粒中心未反應(yīng)區(qū)的擴(kuò)散。在氣-固反應(yīng)固碳過(guò)程中反應(yīng)初始固碳速率快,受到化學(xué)反應(yīng)速率控制;而后隨著新相產(chǎn)物層的形成、長(zhǎng)大,產(chǎn)物層逐漸包裹中心未反應(yīng)區(qū),反應(yīng)開(kāi)始受到擴(kuò)散傳質(zhì)控制,固碳速率開(kāi)始變得緩慢,這也導(dǎo)致干法固碳的固碳量有限[17,20]。由于溫度對(duì)于加快反應(yīng)速率有著重要作用,通過(guò)提高碳化溫度可以起到加快初期碳化速率的效果,因此在高溫下鋼渣干法固碳更為有利[10,22]。
而濕法碳化過(guò)程以水為介質(zhì),碳化過(guò)程包含氣-液-固三相,相比干法碳化的反應(yīng)過(guò)程更加復(fù)雜。水的存在為 CO2氣體的溶解和從鋼渣中浸出鈣離子提供了良好的條件,有助于提高碳化反應(yīng)速率。此外,不需要像干法碳化一樣的高溫,有利于較長(zhǎng)時(shí)間進(jìn)行碳化反應(yīng)[23-24]。濕法碳化反應(yīng)過(guò)程如式(3)~式(5)所示[25]:
CO2+H2O→2H+ +CO3 2- (3)
CaSiO3+2H+ →Ca2++SiO2+H2O (4)
Ca2++CO3 2-→CaCO3 (5)
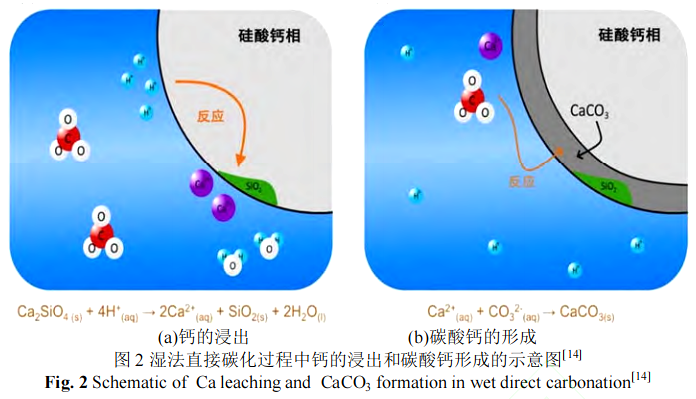
濕法碳化的第一步是 CO2溶入水溶液中,然后 CO2和水反應(yīng)形成碳酸根和氫離子。氫離子從礦物中浸出金屬鈣離子,最后鈣離子和碳酸根離子結(jié)合形成碳酸鈣,完成鋼渣的碳化過(guò)程,反應(yīng)過(guò)程如圖 2 所示。從圖 2 可以看出,碳化反應(yīng)發(fā)生后 CaCO3和 SiO2作為產(chǎn)物層在鋼渣顆粒表面形成,反應(yīng)過(guò)程動(dòng)力學(xué)符合未反應(yīng)核模型[14,18]。產(chǎn)物層形成后,隨后的碳化反應(yīng)過(guò)程如下:1)氣體向液相中的溶解;2)離子穿過(guò)產(chǎn)物層的擴(kuò)散;3)界面反應(yīng)形成碳酸鈣。這是濕法直接碳化反應(yīng)的關(guān)鍵特征,也正是產(chǎn)物層的存在減緩了進(jìn)一步的碳化反應(yīng)速率[26]。
室溫下干法碳化固碳量低且速率慢,不具備固碳優(yōu)勢(shì),而高溫下的干法碳化有利于提高 CO2的擴(kuò)散速率,因此下文主要針對(duì)高溫干法碳化和常規(guī)濕法碳化的影響因素展開(kāi)論述。
2 轉(zhuǎn)爐鋼渣高溫干法碳化的影響因素
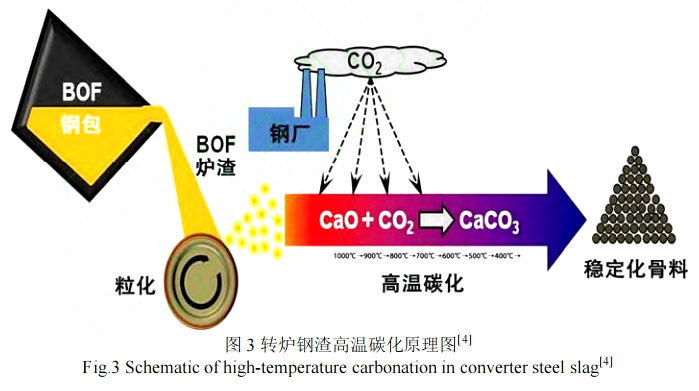
高溫下有利于加快擴(kuò)散傳質(zhì),因而也常用于二氧化碳的捕獲和分離系統(tǒng)中,該系統(tǒng)利用石灰基吸收劑進(jìn)行循環(huán)碳化/煅燒循環(huán),通常在 600~700 ℃進(jìn)行[27-29]。鋼渣從轉(zhuǎn)爐出來(lái)本身就自帶高溫(>500 ℃),這就為鋼渣的高溫干法碳化提供了很好的條件,其碳化處理過(guò)程示意圖如圖 3 所示[4]。
2.1 溫度對(duì)干法固碳的影響
Santos 等人[30]針對(duì)轉(zhuǎn)爐鋼渣的高溫碳化做了深入的探究,選取了 2 組轉(zhuǎn)爐渣 BOFI(自由氧化鈣含量低)、BOFII(自由氧化鈣含量高)和純 CaO,首先在 pCO2=101.325 kPa 的條件下通過(guò) TGA 試驗(yàn)探索了碳化溫度的臨界值在 900 ℃左右,900 ℃以上碳化形成的碳酸鈣會(huì)發(fā)生分解;分析了不同自由氧化鈣含量和不同溫度對(duì)轉(zhuǎn)爐鋼渣碳化增重的影響(如圖4),發(fā)現(xiàn)更高自由氧化鈣含量的鋼渣固碳量更大且固碳速率也更快;在 500~800 ℃,提高溫度,固碳量和固碳速率也會(huì)增加。純 CaO 在碳化初期增重曲線呈線性增加,不同溫度下曲線斜率相差不大,表明初期碳化速率隨溫度變化不大;隨后反應(yīng)性減弱,但溫度越高碳化速率越快(圖 4c)。相比之下,轉(zhuǎn)爐渣由于表面和外孔的快速碳化,碳化剛開(kāi)始時(shí)有著非常短暫的急劇增重(1 min 內(nèi)),之后呈現(xiàn)出速率衰減型趨勢(shì),CO2 緩慢深入滲透到顆粒中進(jìn)行反應(yīng),從而持續(xù)增重(圖 4a,圖 4b)。可以看出,溫度對(duì)轉(zhuǎn)爐渣碳化的影響比對(duì)純CaO 的影響更大,由于純 CaO 樣品的表面有足夠的 CaO 可用于碳化反應(yīng),初期碳化反應(yīng)的進(jìn)行不涉及到 CO2的擴(kuò)散,而不同溫度下純 CaO 樣品初期碳化的增重差異不大,說(shuō)明碳化過(guò)程中溫度對(duì)化學(xué)反應(yīng)的影響不大,此時(shí)想要提高反應(yīng)速率應(yīng)該是加大 CO2 濃度或壓力。結(jié)合轉(zhuǎn)爐渣的增重曲線可知,從促進(jìn)初期碳化反應(yīng)速率來(lái)看,溫度的提升可以很好加快前期碳化速率;從固碳量的角度來(lái)看,溫度對(duì)控制 CO2 擴(kuò)散比控制碳化反應(yīng)對(duì)鋼渣碳化過(guò)程的作用更大,對(duì)于鋼渣而言,表面 CaO 少,碳化增重曲線短暫大幅上升后,表面 CaO消耗完,進(jìn)一步碳化需要 CO2擴(kuò)散至樣品未反應(yīng)區(qū)域內(nèi)進(jìn)行。純 CaO 樣品在碳化一段時(shí)間后,由于碳酸鈣層的形成,CO2 的擴(kuò)散也成為了限制性環(huán)節(jié),反應(yīng)速率逐漸降低。更高溫度下,CO2 的擴(kuò)散速率更快,因而碳化增重量也越大。此外,在加壓加熱的試驗(yàn)條件下,發(fā)現(xiàn)最佳碳化溫度緊緊處于穩(wěn)定碳化和碳酸鹽分解之間的轉(zhuǎn)變溫度之下:在 pCO2=101.325kPa 時(shí),最佳碳化溫度在 830~850 ℃;在 pCO2=20.265 kPa 時(shí),最佳碳化溫度在 750~770 ℃,這是因?yàn)楦叩?CO2 壓力下,碳酸鹽的穩(wěn)定性增加。加壓和通過(guò)蒸汽加濕 CO2 可以促進(jìn)碳化,但是作用不大,因?yàn)閿U(kuò)散限制了樣品中心未反應(yīng)區(qū)自由氧化鈣的轉(zhuǎn)化。通過(guò)提高溫度加快 CO2 的擴(kuò)散速率是行之有效的措施,且鋼鐵生產(chǎn)企業(yè)煙氣中自帶高溫 CO2(pCO2=20.265 kPa),不需要額外的加熱分離或濃縮處理。

2.2 CO2濃度對(duì)干法固碳的影響
Tian 等人研究了在 600 ℃干法固碳過(guò)程中氣氛 CO2濃度對(duì)固碳量的影響,固碳過(guò)程的動(dòng)力學(xué)曲線如圖 5 所示[17]。可以看出,在 1 h 內(nèi)的碳化反應(yīng)動(dòng)力學(xué)曲線的變化趨勢(shì)幾乎是相似的。固碳量隨著 CO2濃度的增加逐漸增加,但是增加的幅度不大。僅僅 CO2體積分?jǐn)?shù)在 100%時(shí)固碳量與另外其他 3 組低濃度的試驗(yàn)有一定差距。當(dāng) CO2體積分?jǐn)?shù)在 5%~100%時(shí),最終的碳化轉(zhuǎn)化率在 45.9%~52.5%內(nèi)波動(dòng)。這為鋼渣干法封存煉鋼廠高溫?zé)煔猓–O2 體積分?jǐn)?shù)在 5%~15%)中的 CO2提供了可能。相比溫度對(duì)鋼渣干法碳化的影響,CO2濃度的影響更小。

2.3 鋼渣顆粒尺寸對(duì)干法固碳的影響
減小鋼渣顆粒尺寸有助于提高鋼渣顆粒比表面、縮短鋼渣碳化過(guò)程的擴(kuò)散距離,從而加快鋼渣碳化。在工業(yè)上實(shí)現(xiàn)對(duì)鋼渣的高溫干法碳化前仍然需要進(jìn)一步的優(yōu)化,盡管高溫下有著良好的碳化反應(yīng)動(dòng)力學(xué)和更快的 CO2擴(kuò)散速率,但是自由氧化鈣的完全轉(zhuǎn)化仍然受到 CO2向鋼渣顆粒內(nèi)部擴(kuò)散的影響,即使在鋼渣顆粒尺寸為 0.08~0.5 mm 的試驗(yàn)中[30],尺寸仍然還需要進(jìn)一步降低來(lái)縮短 CO2的擴(kuò)散距離。其試驗(yàn)使用的鋼渣尺寸已經(jīng)是目前滾動(dòng)造粒設(shè)備的最小尺寸,因此想要獲得更低尺寸的鋼渣顆粒以促進(jìn)自由氧化鈣轉(zhuǎn)化,還有賴于造粒和熱態(tài)球磨技術(shù)的進(jìn)一步發(fā)展。盡管在工藝優(yōu)化的條件下,鋼渣在冷卻過(guò)程中在高溫段經(jīng)歷的時(shí)間畢竟有限,額外的提高鋼渣的能源供應(yīng)也會(huì)加大固碳成本且起不到節(jié)能減排目的,因而結(jié)合生產(chǎn)實(shí)際的高溫干法碳化只是可以充分利用鋼渣余熱和高溫的 CO2 煙氣,并不能最大程度實(shí)現(xiàn)鋼渣的固碳轉(zhuǎn)化。
3 轉(zhuǎn)爐鋼渣濕法碳化的影響因素
溫度、液固比、CO2壓力、鋼渣的粒徑及超聲波等對(duì)鋼渣濕法碳化過(guò)程的固碳速率都有很重要的影響[25, 31-35]。
3.1 溫度對(duì)濕法碳化的影響
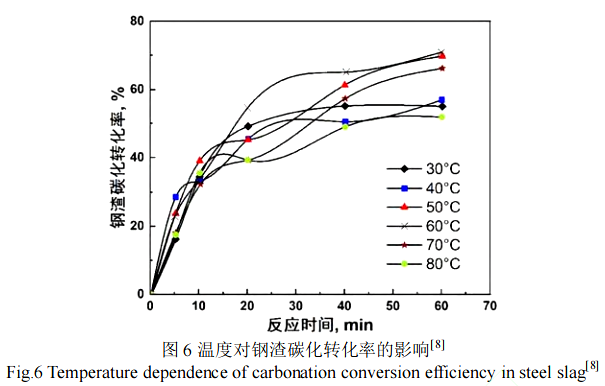
Chang 等人[8]在 30~80 ℃內(nèi)研究了轉(zhuǎn)爐鋼渣在 1 h 內(nèi)固碳轉(zhuǎn)化率的變化,發(fā)現(xiàn)固碳轉(zhuǎn)化率在 60 ℃時(shí)最大,轉(zhuǎn)化率為 72.2%(如圖 6 所示)。溫度對(duì)固碳過(guò)程有著重要的影響,能同時(shí)影響化學(xué)反應(yīng)速率和平衡常數(shù)、CO2 在水溶液中的溶解和鈣離子的浸出過(guò)程。根據(jù)Arrhenius 公式,隨著溫度的增加,反應(yīng)速率常數(shù)呈指數(shù)級(jí)增加,碳化反應(yīng)速率被顯著提高。溫度的增加也可以加快鋼渣顆粒中鈣離子的浸出,但同時(shí)也會(huì)造成 CO2 在溶液中的溶解量降低。因此,溫度對(duì)于固碳轉(zhuǎn)化率的影響有著兩面性。在 60 ℃以下,隨著溫度的增加,由于更高的鈣離子浸出率,固碳轉(zhuǎn)化率提高。而在 60 ℃以上時(shí),隨著溫度的進(jìn)一步增加,由于 CO2在溶液中的溶解量降低,導(dǎo)致固碳轉(zhuǎn)化率下降;在 60~80 ℃,CO2在溶液中的溶解被認(rèn)為是影響碳化過(guò)程的關(guān)鍵因素。
3.2 液固比對(duì)濕法碳化的影響
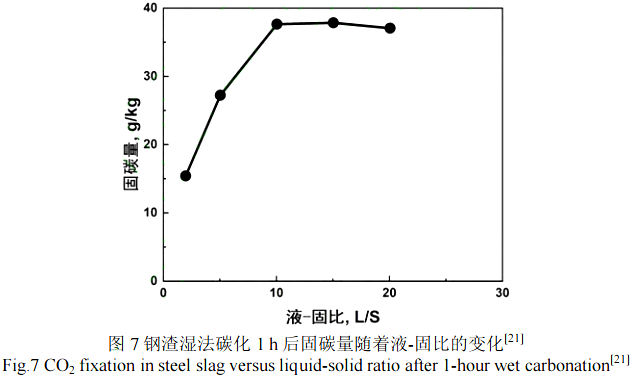
液固比是鋼渣濕法碳化的關(guān)鍵參數(shù)之一,是指單位質(zhì)量的鋼渣所使用液體的體積(L/kg)。水的存在對(duì)濕法碳化過(guò)程中 CO2的溶解和其在水中的擴(kuò)散以及鋼渣中金屬離子的浸出有著至關(guān)重要的影響[14]。Kurusta 等人[36]研究了水在鋼渣碳化反應(yīng)中的作用,發(fā)現(xiàn)相比干法碳化,濕法碳化的固碳量是干法的 3 倍。Revathy 等人[21]研究了液固比在 0~30 內(nèi)對(duì)鋼渣濕法碳化 1 h 后固碳量的影響,如圖 7 所示。隨著液-固比的增加,固碳量先增加,而后減小。低固液比條件下 CO2的溶解量有限,同時(shí)也不利于鈣的浸出,但水含量過(guò)高會(huì)導(dǎo)致液體中溶解的 CO2的濃度和浸出的金屬離子的濃度降低,同時(shí)也會(huì)阻礙氣體分子在渣漿中的擴(kuò)散,導(dǎo)致碳化速率和固碳量降低[23]。
3.3 CO2壓力對(duì)濕法碳化的影響
CO2 壓力對(duì)于其在溶液中的溶解度有很大影響,增加壓力有助于提高溶液中 CO2 的溶解量。當(dāng) CO2 壓力低于臨界值時(shí),鈣的浸出和固碳量明顯降低,主要是因?yàn)槿芤褐腥芙獾腃O2 量不夠。此時(shí),CO2 的溶解是碳化反應(yīng)的限制性環(huán)節(jié)時(shí),增加 CO2 壓力可以起到促進(jìn)鋼渣碳化的作用,已有研究表明增加 CO2 分壓可以顯著提高鋼渣的碳化程度和固碳量。但當(dāng) CO2 壓力超過(guò)臨界值時(shí),CO2 壓力對(duì)碳化過(guò)程的影響不大,說(shuō)明 CO2 的傳質(zhì)不是碳化反應(yīng)的限制性環(huán)節(jié)。此時(shí),鈣離子的浸出成為碳化過(guò)程的限制性環(huán)節(jié),CO2 壓力的影響減弱[25,37-38]。過(guò)高的 CO2壓力也會(huì)導(dǎo)致碳化礦相的快速析出長(zhǎng)大,在鋼渣表面形成碳化產(chǎn)物層,阻礙鋼渣內(nèi)部未反應(yīng)區(qū)的進(jìn)一步碳化[37]。吳昊澤等人[35]發(fā)現(xiàn) CO2壓力遞增比在單一CO2壓力下的碳化效果更好,因此在濕法碳化過(guò)程中可以采用遞進(jìn)式增加 CO2壓力。
3.4 鋼渣的粒徑和超聲處理對(duì)濕法碳化的影響
Huijgen 等人[25]研究發(fā)現(xiàn)在加水量(液固比)、溫度、CO2壓力等條件處于最優(yōu)條件時(shí),鈣從鋼渣顆粒中的浸出是碳化反應(yīng)的限制性環(huán)節(jié),即鈣從鋼渣內(nèi)部向表面的擴(kuò)散是限制性環(huán)節(jié)。對(duì)反應(yīng)產(chǎn)物層形貌和顯微結(jié)構(gòu)進(jìn)行分析發(fā)現(xiàn),在硅酸鈣碳化反應(yīng)后形成貧鈣的二氧化硅區(qū)和析出的碳酸鈣顆粒包覆在未反應(yīng)的硅酸鈣表面(如圖 8 所示),這嚴(yán)重阻礙了鈣從未反應(yīng)的硅酸鈣相向鋼渣顆粒表面的擴(kuò)散傳遞。減小反應(yīng)產(chǎn)物層厚度是最為行之有效的措施,有兩條路徑,其一是減小鋼渣顆粒尺寸以達(dá)到縮短鈣浸出過(guò)程的擴(kuò)散距離,研究表明減少鋼渣顆粒尺寸可以極大程度提高碳化速率和固碳量,當(dāng)鋼渣尺寸從小于 2 000 μm減小到小于 38 μm 時(shí),鋼渣中鈣的碳化率從約 26%增加到 74%[25]。第二條路徑則是破壞或去除產(chǎn)物層,利用超聲波可以加快濕法碳化過(guò)程的速率并提高固碳量[39],其機(jī)理就是通過(guò)超聲波去除阻礙傳質(zhì)的鈍化層(析出的碳酸鈣顆粒和殘余二氧化硅)來(lái)實(shí)現(xiàn)增強(qiáng)碳化的目的,并且已經(jīng)通過(guò)鋼渣尺寸的變化得到證明,其原理路線如圖 9 所示。在只有攪拌的碳化過(guò)程中,碳化顆粒的尺寸是增加的;而在使用超聲波的條件下,碳化顆粒產(chǎn)物層被打碎,碳化顆粒尺寸減小,從而增強(qiáng)了鋼渣的碳化,但是該過(guò)程需要對(duì)超聲波參數(shù)進(jìn)行優(yōu)化,避免大的能量消耗。

4 結(jié) 語(yǔ)
1)鋼渣的高溫碳化過(guò)程主要的限制性環(huán)節(jié)是 CO2穿過(guò)產(chǎn)物層向鋼渣內(nèi)部未反應(yīng)區(qū)域的擴(kuò)散,提高溫度可以增加 CO2 的擴(kuò)散速率,最佳碳化溫度僅僅低于穩(wěn)定碳化和碳酸鹽分解之間的轉(zhuǎn)變溫度,減小鋼渣尺寸可以縮短 CO2 擴(kuò)散路徑,因此對(duì)高溫干法碳化十分有利。
2)濕法碳化的主要限制環(huán)節(jié)是鋼渣中鈣從內(nèi)部向鋼渣表面的擴(kuò)散,在對(duì)加水量(液固比)、溫度、CO2 壓力和攪拌速率等條件優(yōu)化后,減小鋼渣尺寸和利用超聲波震蕩能有效加快擴(kuò)散。
3)由于鋼渣從轉(zhuǎn)爐出來(lái)后具有較高的溫度,且單一的碳化方式都有其局限,可考慮將兩種固碳方式結(jié)合使用,首先在高溫鋼渣冷卻過(guò)程中利用鋼渣余熱進(jìn)行高溫干法碳化,并降低鋼渣顆粒尺寸從而提高固碳量和鈣的轉(zhuǎn)化率;通過(guò)干法碳化固定一部分鈣,減輕濕法碳化任務(wù),有利于縮短濕法碳化時(shí)間,待鋼渣高溫碳化結(jié)束經(jīng)球磨后再進(jìn)行濕法碳化,結(jié)合尺寸優(yōu)化和超聲波的利用,實(shí)現(xiàn)鋼渣最大程度的碳化;該過(guò)程充分利用了鋼渣自身?xiàng)l件,能更有效發(fā)揮出鋼渣固碳的優(yōu)勢(shì),有利于固廢資源和能量的高效分級(jí)利用。
[參考文獻(xiàn)]
[1] 郭英楠. 大氣二氧化碳濃度達(dá)歷史頂點(diǎn)[J]. 生態(tài)經(jīng)濟(jì), 2019, 35 (7): 5-8.
[2] 劉政陽(yáng), 李挺宇. 全球氣候變暖趨勢(shì)急劇加速[J]. 生態(tài)經(jīng)濟(jì), 2019, 35 (9): 1-4.
[3] 韓敏, 俞金香.碳捕獲與封存技術(shù)法律規(guī)制的現(xiàn)狀及問(wèn)題研究[J]. 蘭州大學(xué)學(xué)報(bào)(社會(huì)科學(xué)版), 2015, 43(3): 95-101.
[4] BODOR M, SANTOS R M, GERVEN T V, et al. Recent developments and perspectives on the treatment of industrial wastes by mineral carbonation-a review[J]. Central European Journal of Engineering, 2013, 3(4): 566-584.
[5] LACKNER K S. A guide to CO2 sequestration[J]. Science, 2003, 300(5626): 1677-1678.
[6] SEIFRITZ W. CO2 disposal by means of silicates[J]. Nature, 1990, 345(6275): 486.
[7] XUE Yongjie, WU Shaopeng, HOU Haobo, et al. Experimental investigation of basic oxygen furnace slag used as aggregate in asphalt mixture[J]. Journal of Hazardous Materials, 2006, 138(2): 261-268.
[8] CHANG E E, CHEN C H, CHEN Y H, et al. Performance evaluation for carbonation of steel-making slags in a slurry reactor[J]. Journal of Hazardous Materials, 2011, 186(1): 558-564.
[9] WANG G, WANG Y H, GAO Z L. Use of steel slag as a granular material: Volume expansion prediction and usability criteria[J]. Journal of Hazardous Materials, 2010, 184(1/2/3): 555-560.
[10] BOBICKI E R, LIU Qingxia, XU Zhenghe, et al. Carbon capture and storage using alkaline industrial wastes[J]. Progress in Energy and Combustion Science, 2012, 38(2): 302-320.
[11] ELONEVA S, TEIR S, SALMINEN J, et al. Steel converter slag as a raw material for precipitation of pure calcium carbonate[J]. Industrial & Engineering Chemistry Research, 2008, 47(18): 7104-7111.
[12] ELONEVA S, TEIR S, REVITZER H, et al. Reduction of CO2 emissions from steel plants by using steelmaking slags for production of marketable calcium carbonate[J]. Steel Research International, 2009, 80(6): 415-421
[13] ELONEVA S, MANNISTO P, SAID A, et al. Ammonium salt-based steelmaking slag carbonation: Precipitation of CaCO3 and ammonia losses assessment[J]. Greenhouse Gases Science & Technology, 2011, 1(4):305-311.
[14] DIGIOVANNI C, HISSEINE O A, AWOLAYO A N. Carbon dioxide sequestration through steel slag carbonation: Review of mechanisms, process parameters, and cleaner upcycling pathways[J]. Journal of CO2 Utilization, 2024, 81.DOI:10.1016/j.jcou.2024.102736.
[15] 劉文昊, 陳慶彩, 徐騰飛. 雙碳戰(zhàn)略背景下的鋼渣固碳技術(shù)研究進(jìn)展[J]. 環(huán)境工程, 2024, 42(5): 172-182.
[16] 王愛(ài)國(guó), 何懋燦, 莫立武,等. 碳化養(yǎng)護(hù)鋼渣制備建筑材料的研究進(jìn)展[J]. 材料導(dǎo)報(bào), 2019, 33(9): 2939- 2948.
[17] TIAN Sicong,JIANG Jianguo,CHEN Xuejing, et al. Direct gas-solid carbonation kinetics of steel slag and the contribution to in situ sequestration of flue gas CO2 in steel-making plants[J]. ChemSusChem, 2013, 6(12): 2348-2355.
[18] GAO Zihe, ZHAO Qing, TAO Mengjie, et al. Recent research progress on the direct carbon capture of steel slag to prepare building materials[J]. Green and Smart Mining Engineering, 2024, 1(4): 387-395.
[19] MYERS C A, NAKAGAKI T, AKUTSU K. Quantification of the CO2 mineralization potential of ironmaking and steelmaking slags under direct gas-solid reactions in flue gas[J]. International Journal of Greenhouse Gas Control, 2019, 87: 100-111.
[20] BHATJA S K, PERLMUTTER D D. Effect of the product layer on the kinetics of the CO2-lime reaction[J]. AIChE Journal, 1983, 29(1): 79-86.
[21] REVATHY T D R, PALANIVELU K, RAMACHANDRAN A, et al. Direct mineral carbonation of steelmaking slag for CO2 sequestration at room temperature[J]. Environmental Science and Pollution Research, 2016, 23(8): 7349-7359.
[22] WANG JUNYA, ZHONG MI, WU PENGFEI, et al. A review of the application of steel slag in CO2 fixation[J]. ChemBioEng Reviews, 2021, 8(3): 189-199.
[23] COSTA G, BACIOCCHI R, POLETTINI A, et al. Current status and perspectives of accelerated carbonation processes on municipal waste combustion residues[J]. Environmental Monitoring and Assessment, 2007, 135(1/2/3): 55-75.
[24] THONEMANN N, ZACHAROPOULOS L, FROMME F, et al. Environmental impacts of carbon capture and utilization by mineral carbonation: a systematic literature review and meta life cycle assessment[J]. Journal of Cleaner Production, 2022, 332.DOI:10.1016/j.jclepro.2021.130067.
[25]HUIJGEN W J J,WITKAMP G J,COMANS R N J.Mineral CO2 sequestration by steel slag carbonation[J].Environmental science & technology, 2005, 39(24):9676-9682.
[26] KIM J, AZIMI G. The CO2 Sequestration by supercritical carbonation of electric arc furnace slag[J]. Journal of CO2 Utilization, 2021, 52.DOI:10.1016/j.jcou.2021.101667.
[27] REDDY E P,SMIRNIOTIS P G .High-temperature sorbents for CO2 made of alkali metals doped on CaO supports[J].Journal of Physical Chemistry B, 2004, 108(23):7794-7800.
[28] BLARNEY J, ANTHONY E J, WANG J, et al. The calcium looping cycle for large-scale CO2 capture[J]. Progress in Energy and Combustion Science, 2010, 36(2): 260-279.
[29] MANOVIC V, ANTHONY E J. Lime-based sorbents for high-temperature CO2 capture—a review of sorbent modification methods[J]. International Journal of Environmental Research and Public Health, 2010, 7(8): 3129-3140.
[30] SANTOS R M, LING D, SARVARAMINI A, et al. Stabilization of basic oxygen furnace slag by hot-stage carbonation treatment[J]. Chemical Engineering Journal, 2012, 203(1): 239-250.
[31] 涂茂霞, 雷澤, 呂曉芳, 等. 水淬鋼渣碳酸化固定 CO2[J]. 環(huán)境工程學(xué)報(bào), 2015, 9(9): 4514-4518.
[32] 儲(chǔ)健. 轉(zhuǎn)爐鋼渣碳化磚的試驗(yàn)研究初探[J]. 粉煤灰, 1998(2): 26-28.
[33] 吳昊澤, 張林菊, 葉正茂, 等. 水分對(duì)鋼渣碳化的影響[J]. 濟(jì)南大學(xué)學(xué)報(bào)(自然科學(xué)版), 2009, 23(3): 221- 224.
[34] 張豐, 莫立武, 鄧敏. 碳化 MgO-CaO-粉煤灰-水泥四元組分制備砂漿的強(qiáng)度和微觀結(jié)構(gòu)[J]. 硅酸鹽學(xué)報(bào), 2015, 43(8): 1032-1039.
[35] 吳昊澤, 徐東宇, 梁曉杰. CO2壓力對(duì)碳化養(yǎng)護(hù)鋼渣制備建筑材料的影響[J]. 商品混凝土, 2020(6): 36-38.
[36] KURUSTA T, MUCSI G, KUMAR S, et al. Carbon-dioxide sequestration by mechanical activation of Linz Donawitz steel slag; the effect of water on CO2 capture[J]. Fuel, 2023, 352.DOI: 10.1016/j.fuel.2023.128951.
[37] WANG Shuping, WANG Mingda, LIU Fang, et al. A Review on the Carbonation of Steel Slag: Properties, Mechanism, and Application[J]. Materials, 2024, 17(9): 2066.DOI: 10.3390/ma17092066
[38] CHEN Zhaohou,CANG Zhizhi,YANG Fengmin,et al.Carbonation of steelmaking slag presents an opportunity for carbon neutral: A review[J]. Journal of CO2 Utilization, 2021, 54. DOI:10.1016/j.jcou.2021.101738.
[39] SANTOS R M, FRANÇOIS D, MERTENS G, et al. Ultrasound-intensified mineral carbonation[J]. Applied Thermal Engineering, 2013, 57(1/2): 154-163.
